Вставка всего одного нуклеотида в регуляторный участок ДНК привела к полному переключению пола у мышей: генетические самки с XX-хромосомами развились как самцы — с семенниками и мужскими гениталиями. Исследование, опубликованное в журнале Nature Communications 9 апреля 2026 года, показало, что для запуска мужского развития не обязательно менять сами гены — достаточно мельчайшего изменения в участке ДНК, который этими генами управляет. Результат настолько впечатляет, что заставляет пересмотреть многие представления о генетике пола.

Изменения в определенном участке ДНК самок мышей изменили процесс их развития таким образом, что у них сформировались мужские половые органы.
Как определяется пол у млекопитающих: роль генов SRY и SOX9
Пол млекопитающих определяется на эмбриональной стадии, и ключевую роль в этом процессе играют два гена — SRY и SOX9. Ген SRY находится на Y-хромосоме: он производит белок, который «включает» второй ген — SOX9. Активация SOX9 запускает цепную реакцию, которая ведёт к формированию семенников и мужских половых клеток. Если SOX9 остаётся выключенным — развиваются яичники, и эмбрион идёт по женскому пути.
Но у SOX9 есть нечто вроде дистанционного пульта управления — участок некодирующей ДНК под названием Enh13 (от слова enhancer — «усилитель»). Этот фрагмент длиной всего 557 пар оснований расположен за сотни тысяч пар от самого гена SOX9, но именно он решает, будет ли ген активен. Белок SRY «садится» на этот переключатель и запускает SOX9 в работу.
Важно, что Enh13 — это не ген, он не кодирует никаких белков. Он относится к так называемой некодирующей «мусорной» ДНК, которая составляет около 98% генома. Долгое время её называли «мусорной», но сейчас становится ясно, что она играет огромную роль в регуляции работы генов.
Учёные оживили замороженный мозг мыши. В будущем мы сможем воскрешать людей?
Как одна мутация ДНК меняет пол мыши
Команда под руководством доктора Нитцан Гонен из Университета Бар-Илан (Израиль) использовала технологию CRISPR для редактирования Enh13 у мышиных эмбрионов. С помощью молекулярных «ножниц» учёные внесли минимальную мутацию — вставили одну-единственную букву (нуклеотид) в этот регуляторный участок.
Результат оказался поразительным. Мыши с XX-хромосомами — то есть генетические самки — развились как самцы: у них сформировались семенники и мужские наружные половые органы. Как отметила Нитцан Гонен: «Одна буква ДНК из примерно 2,8 миллиарда — и этого хватило, чтобы полностью изменить путь развития».
Помимо вставки одного нуклеотида, команда провела параллельный эксперимент с удалением трёх букв в том же участке Enh13. Обе мутации привели к развитию семенников у XX-мышей, хотя вставка одного нуклеотида дала более выраженный эффект.

Лабораторные мыши — основная модель для изучения генетики пола у млекопитающих
При этом для переключения пола мутация должна была затронуть обе копии Enh13 — ведь у каждой клетки две копии 17-й хромосомы, на которой расположен этот участок. Если мутация была только в одной копии, самки развивались нормально, с яичниками и без каких-либо мужских признаков.
Что такое Enh13 и как он влияет на определение пола
Предыдущие работы той же группы уже показали, что Enh13 критически важен для мужского развития. В 2018 году учёные обнаружили, что полное удаление Enh13 приводит к обратному эффекту: мыши с XY-хромосомами (генетические самцы) развивались как самки. Без этого переключателя активность SOX9 падала примерно на 80%, и вместо семенников формировались яичники.
Новое исследование раскрыло вторую сторону Enh13 — его роль в подавлении мужского пути у самок. Оказалось, что в норме на Enh13 «садятся» белки-репрессоры (такие как RUNX1, NR5A1 и GATA4), которые блокируют SOX9 в женских эмбрионах. Когда мутация нарушает работу этих репрессоров, SOX9 активируется даже без белка SRY — того самого, что обычно запускает мужское развитие.
Учёные описывают Enh13 как своеобразное «поле битвы полов»: на этом участке ДНК конкурируют белки, продвигающие мужской путь развития, и белки, поддерживающие женский. Итог этой молекулярной борьбы определяет, станет ли эмбрион самцом или самкой. А мутация длиной в одну букву может решительно сдвинуть баланс.
Еще больше познавательных материалов вы найдете в нашем Telegram-канале. Обязательно подпишитесь!
Ещё один важный нюанс: SOX9 способен поддерживать и усиливать собственную активность по принципу обратной связи. Поэтому даже минимальная «утечка» активации — когда репрессоры перестают работать — запускает самоподдерживающуюся петлю усиления гена. Авторы исследования отмечают, что даже небольшой начальный импульс достаточен для запуска полной цепочки мужского развития.
Как мутации ДНК мышей связаны с генетикой человека
Человек и мышь — далеко не близнецы, но генетически мы гораздо ближе, чем может показаться. По разным оценкам, геномы человека и мыши совпадают примерно на 85%, а если сравнивать только гены, кодирующие белки, сходство достигает 80–99% в зависимости от метода подсчёта. Именно поэтому мыши остаются главной моделью в генетике и медицине.
Участок Enh13, изученный в этом исследовании, имеет прямой аналог в геноме человека. Более ранние работы показали, что удаление этого участка у человека тоже приводит к реверсии пола у XY-индивидов, а его дупликация (удвоение) связана с развитием мужских признаков у XX-индивидов.
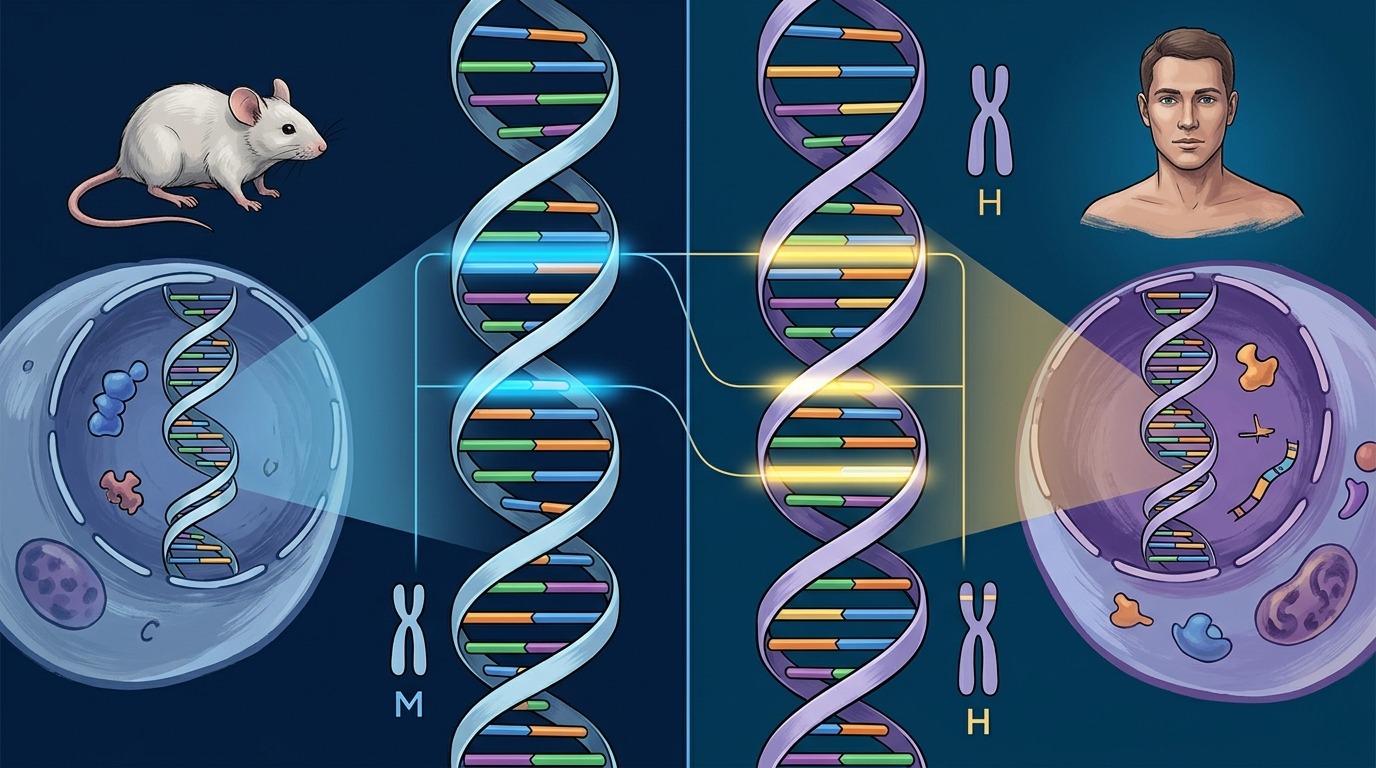
Сравнение геномов мыши и человека показывает высокое сходство ключевых регуляторных участков
Это делает результаты исследования потенциально важными для понимания нарушений полового развития у людей. Эти состояния встречаются примерно у 1 из 4500–5500 новорождённых и проявляются несоответствием между хромосомным набором и анатомическими половыми признаками. Более половины случаев нарушения полового развития до сих пор не получают генетического диагноза — во многом потому, что стандартные генетические тесты анализируют только белок-кодирующие гены, составляющие лишь 1,5% всей ДНК.
Впрочем, пока речь идёт только о мышиной модели. Механизмы активации Enh13 могут частично отличаться у человека и мыши, и для клинических выводов нужны дополнительные исследования.
Некодирующая ДНК: как она управляет работой генов
Одно из главных следствий этой работы — очередное доказательство того, что «мусорная ДНК» — это не мусор. 98% нашего генома не кодируют белки, но содержат тысячи регуляторных элементов — энхансеров, сайленсеров, промоторов, — которые управляют тем, когда, где и насколько интенсивно работают гены.
Элишева Абберболк, доктор Университета Бар-Илан и ведущий автор статьи, подчеркнула: недостаточно смотреть только на гены. Мутации, вызывающие заболевания, могут скрываться в некодирующем геноме — в участках ДНК, которые контролируют активность генов, а не кодируют белки. В этом смысле особенно важны и новые инструменты борьбы с мутациями, рассчитанные на точечную работу с ошибками в ДНК.
Если хотите обсудить новость с другими читателями, заходите в наш Telegram-чат!
Команда Гонен считает, что Enh13 — это лишь начало. По их словам, в геноме вероятно существуют сотни подобных регуляторных элементов, мутации в которых могут объяснять не только нерасшифрованные случаи DSD, но и другие генетические заболевания, причины которых пока неизвестны.
Эта работа не просто дополняет учебник по генетике пола — она сдвигает фокус внимания с генов на их регуляторы. Если одна буква в участке ДНК, который даже не производит белок, способна полностью изменить развитие организма — значит, чтобы по-настоящему понять геном, недостаточно читать только его «инструкции». Нужно разобраться в том, кто и как эти инструкции включает и выключает.




Новости, статьи и анонсы публикаций
Чат с читателямиСвободное общение и обсуждение материалов