Даже у абсолютно здоровых людей в клетках прячутся вирусы, причем иногда годами и десятилетиями. Они не вызывают симптомов, но и не исчезают: просто затаиваются, ускользая от иммунной системы. Новое масштабное исследование показало, какие именно участки человеческого генома определяют, насколько хорошо организм держит эти скрытые инфекции под контролем, и почему у одних людей они остаются безобидными, а у других приводят к серьезным заболеваниям. К таким вирусам можно отнести герпес, который невозможно излечить полностью.
Латентные вирусы прячутся внутри клеток, оставаясь невидимыми для иммунной системы
Что такое латентные вирусы
Когда мы говорим о вирусной инфекции, обычно представляем температуру, кашель и постельный режим. Но существует целый класс вирусов, которые работают иначе. Они проникают в клетки, встраиваются в них, и замолкают. Такие инфекции называют латентными: вирус присутствует в организме, но не размножается активно и не вызывает симптомов.
Классический пример — вирус Эпштейна-Барр (EBV), который есть у подавляющего большинства взрослых людей на планете. Или вирус герпеса HHV-7, который почти все подхватывают еще в детстве. Еще есть анелловирусы — они обнаруживаются у 80–90% населения, но ученые до сих пор точно не знают, как именно они влияют на здоровье.
Все эти вирусы объединяет одна черта: иммунная система не может полностью их уничтожить. Она лишь сдерживает их, не давая размножаться. И именно от того, насколько эффективно работает это сдерживание, зависит, останется ли вирус безобидным попутчиком, или когда-нибудь даст о себе знать болезнью. Герпес, например, может поразить мозг человека.
Что такое вирусная нагрузка у человека
Команда ученых проанализировала данные образцов крови и слюны более чем 917 000 человек из трех крупных медицинских баз данных. Исследователи искали фрагменты вирусной ДНК в биоматериалах здоровых людей — тех, у кого инфекция не перешла в болезнь.
Для каждого участника рассчитали так называемую вирусную нагрузку — количество вирусного генетического материала, циркулирующего в организме. Этот показатель говорит о двух вещах одновременно: какие именно вирусы присутствуют и насколько хорошо иммунная система справляется с их подавлением. Чем выше вирусная нагрузка, тем хуже организм контролирует инфекцию.
Затем исследователи сопоставили уровни вирусной нагрузки с генетическими данными участников, чтобы найти участки ДНК, которые влияют на способность организма держать вирусы в узде.
Еще больше познавательных статей вы найдете в нашем Дзен-канале. Нас уже более 150 000 человек!
Что такое главный комплекс гистосовместимости
Результат оказался впечатляющим: ученые обнаружили 82 конкретных локуса (участка) в человеческом геноме, связанных с уровнем вирусной ДНК в организме. Особенно много таких участков оказалось в так называемом главном комплексе гистосовместимости (МНС) — это область генома, которую можно назвать центром управления иммунной системой.
MHC отвечает за то, как иммунные клетки распознают «своих» и «чужих». Если определённые участки MHC работают менее эффективно, вирусу проще спрятаться и избежать уничтожения. По сути, генетика конкретного человека определяет, насколько «удобным убежищем» его клетки будут для латентных вирусов.
Но генетика — не единственный фактор. Исследование показало, что вирусная нагрузка зависит также от возраста, пола и даже от того, курит ли человек. Большинство изученных вирусов оказались более распространены у мужчин по сравнению с женщинами.

Главный комплекс гистосовместимости — ключевая область генома, управляющая иммунным ответом на вирусы
Как один спящий вирус запускает разные болезни
Одно из самых интересных открытий касается вируса Эпштейна — Барр. Его вирусная нагрузка, как выяснилось, растет с возрастом, причем увеличивается зимой и снижается летом. А вот вирус герпеса HHV-7, наоборот, начинает убывать примерно с середины жизни.
Используя метод менделевской рандомизации (статистический инструмент, который позволяет отделить причинно-следственные связи от простых совпадений), ученые проверили, как вирусная нагрузка связана с конкретными заболеваниями.
Выяснилось, что высокая вирусная нагрузка EBV — прямой фактор риска развития лимфомы Ходжкина (рак лимфатической системы). Это важная находка: она означает, что противовирусные препараты теоретически могли бы снизить риск этого вида рака. Правда, эту идею еще предстоит проверить в клинических испытаниях.
А вот с рассеянным склерозом ситуация оказалась сложнее. EBV давно считается одним из триггеров рассеянного склероза, но связь между количеством вируса и риском РС в этом исследовании не подтвердилась. Это значит, что дело не в том, сколько вируса в организме, а в том, как именно иммунная система на него реагирует. Иммунный ответ, а не сам вирус, может запускать аутоиммунный процесс.
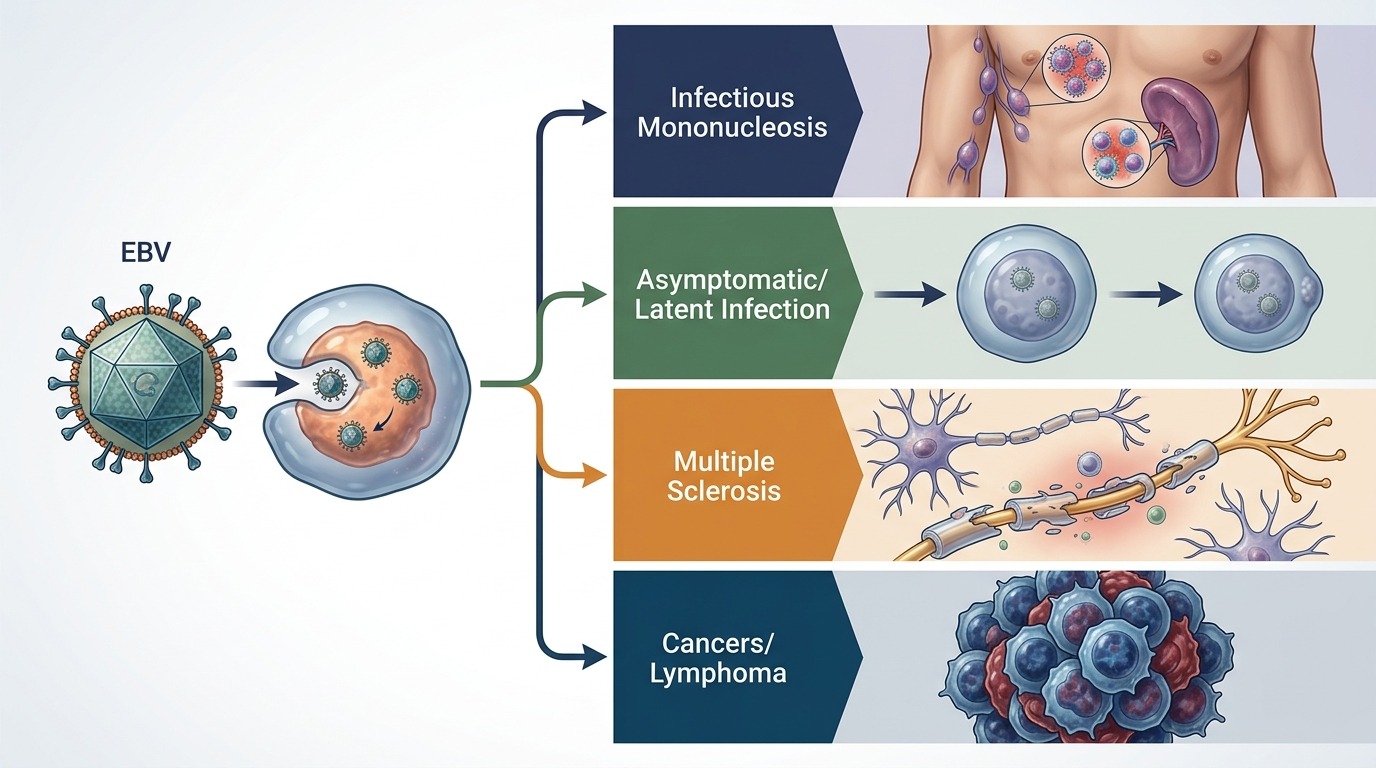
Один и тот же вирус Эпштейна — Барр может приводить к разным последствиям в зависимости от генетики и иммунного ответа
Что ученые пока не знают о вирусах
При всей масштабности работа имеет важное ограничение: исследователи изучали только ДНК-содержащие вирусы — те, что прячутся внутри ДНК клеток. РНК-вирусы, к которым относятся, например, коронавирусы, работают по-другому и в это исследование не вошли.
Кроме того, есть еще одна категория вирусных «жителей» нашего тела: древние вирусы, которые встроились в геном человека тысячи и миллионы лет назад. Они давно утратили способность размножаться, но их генетические следы до сих пор влияют на здоровье — иногда самым неожиданным образом, вплоть до воздействия на предрасположенность к зависимостям.
«Поразительно, как много ДНК может рассказать нам о динамических биологических процессах и о том, как наши привычки, гены и биология формируют эти процессы», — говорит генетик Стивен Маккэрролл, один из авторов исследования.
Это исследование открывает дорогу к персонализированной медицине вирусных инфекций. Если мы знаем, какие генетические особенности делают человека более уязвимым перед конкретным латентным вирусом, можно заранее оценивать риски — и, возможно, предотвращать болезни, которые эти вирусы способны вызвать спустя годы тихого присутствия в организме.




Новости, статьи и анонсы публикаций
Чат с читателямиСвободное общение и обсуждение материалов